Atom ve atomun yapısı
Atom ve atomun yapısı?
Elementlerin tüm özelliğini gösteren en küçük parçasına atom denir. Atom tüm maddenin kimyasal ve fiziksel niteliklerini taşır. Maddeyi meydana getiren atomlar sürekli olarak hareket ederler. Genellikle atomların titreşim hızı saniyede 400 metre kadardır. Bu hız sıcaklıkla ilgilidir. Sıcaklık azaldıkça atomların hızı da azalır. –273 derece de tamamen durur. Bu ısı derecesine saltık sıfır (mutlak sıfır) denir.
Atomun Yapısı
Atomu meydana getiren parçacıklar farklı yüklere sahiptir. Atomda bulunan yükler; negatif yükler ve pozitif yüklerdir. Atomu meydana getiren parçacıklar:
- Cisimden cisme elektrik yüklerini taşıyan negatif yüklü elektron,
- Elektronların yükünü dengeleyen aynı sayıda ama pozitif yüklü olan proton,
- Elektrik yükü taşımayan nötr parçacık nötron
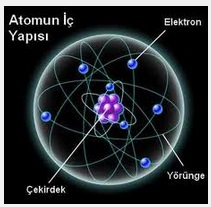
Atomun iç yapısı;
Atomun, değişik durumlarda ortaya çıkan bir çok parçacıkları vardır bunlar; Positon, Meson, Neutrino, Deuteron, Triton, Alfa zerrecikleri, Gama ışınları.
Atom iki bölümden meydana gelir;
- Çekirdek (merkez)
- Katmanlar (yörünge; enerji düzeyi)
Çekirdek, hacim olarak küçük olmasına rağmen, atomun tüm kütlesini meydana getirir. Çekirdekte proton ve nötronlar vardır. Elektronlar ise çekirdek çevresindeki katmanlarda bulunur.
| Tanecik adı | Sembol | Elektrik yükü | Kütle kg |
| Proton | P+ | + | 1,6725.10-27 kg |
| Elektron | e¯ | – | 9,107.10-31 kg |
| Nötron | n0 | 0 | 1,6748.10-27 kg |
Elektronların çekirdek çevresinde dönme hızı, 2,18.108 cm/sn’dir. Elementlerin çekirdekte bulunan protonlar, atomun ( o elementin) tüm kimyasal ve fiziksel özelliklerini belirler.
- Protonlar atomun çekirdeğini oluşturan elemanlardır. Protonlar pozitif elektrik yüklü bir parçacıklardır. Elektronların yükünü dengeler. Ağırlığı; elektrondan fazladır. Sadece taşıdığı elektirik yükünün miktarı elektron ile aynıdır. Atomların cinslerine göre çekirdeklerindeki proton sayısı değişmektedir. Proton sayısı atomlar (elementler) için ayırt edici özelliktir. Yani proton sayısının farklı olması elementin diğerinden farklı olduğu anlamına gelir.
- Nötron, elektirik yükü olmayan nötr parçacıktır. Atom çekirdeklerinde nötronlar vardır. Protondan daha ağırlardır. Nötronların sayıları atomun cinsine göre değişmektedir.
- Elektronların bulunma olasılığının olduğu bölgelere elektron bulutu denir. Merkezde atom çekirdeği bulunur. Elektronlar tek tek bulut meydana getirirler. Elektron bulutu bir küre meydan getirir.
- Kimyasal olaylarda (reaksiyonlarda) yalnızca elektron sayısı değişir. Proton ve nötron, çekirdekte bulunduğu için sayıları değişmez.
- Nötr bir atom için; elektron sayısı= proton sayısı
- (A.N.) Atom numarası= proton sayısı
- Çekirdek yükü= proton sayısı
- İyon yükü= proton sayısı – elektron sayısı (E.S.)
- (K.N.) Kütle numarası= proton + (N.S)nötron sayısı (Nükleon sayısı)(atom ağırlığı)
- Atom Numarası = Proton Sayısı = Çekirdek Yükü = Elektron Sayısı
Atomun Yapısına Göre İletken ve Yalıtkan Nedir?
Elementlerin özelliklerini atomların son yörüngesindeki elektron sayıları belirlemektedir. Elektrikte kullanılan maddelere; yalıtkan, iletken, yarı iletken madde denilir. Atomların dış (serbest) yörüngelerinde elektron sayıları (1-2-3) yani dörtten az olan elementlere iletken denir. İletken malzemelerde örneğin; altın, gümüş, bakır ve alüminyum vs gibi elektronlar atomlarından ayrılıp hareket edebilirler. Bunlar serbest elektronlardır. İletkenler üzerindeki serbest elektronlar elektrik akımını bir noktadan bir noktaya kolaylıkla taşırlar. Bütün metaller iletkendir. Vücudumuzda iyi bir iletkendir. İyonlara sahip sıvılar da iletkendir ve bunlara elektrolit denir. İçtiğimiz su iletkenlik, saf su yalıtkandır. Toprağın içinde su olduğundan iletkendir. Gazlar ise yalıtkandır, ama iyonlarına ayrışan gazlar iletkendir.
Yalıtkan
Elektrik akımını iletmeyen maddelere yalıtkan maddeler adı verilir. Yalıtkanlar elektrik akımını iletmezler. Elektron sayıları 5-6-7 olan elementler ise bir yere kadar yalıtkan sayılır. Yalıtkan maddelerde serbest (valans) elektronlar çok azdır. Yalıtkan maddelere örnek verirsek; kauçuk, hava, yağ, tahta, plastik ve camdır. Değerlik elektronları atomlara sıkıca bağlanmıştır. Bu malzemelerde elektronlar hareket etmezler. Bu maddelerin değerlik elektron sayıları 8 veya 8 ‘e yakın sayıda olduğu için atomdan uzaklaştırılmaları zordur.
Yarı İletken
Elektrik iletkenliği bakımından iletken ile yalıtkan arasında kalan maddelere denir. Dış yörüngelerinde atomların elektron sayıları dört olan elementlere yarı iletken denir. Örneğin germanyum, silisyum gibi maddeler yarı iletkendir.
Elektrik Yükü ve Birimi
Atomun yapısını oluşturan proton ve elektronların elektriksel özellikleri birbirlerine tezattır. Proton (+)yüklü, elektron (-) yüklüdür. Nötronlarsa yüksüzdür. Elektrik yükü Q ya da q ile, birimi coulomb ise C ile gösterilmektedir. Proton ve elektron sayıları bir atomda eşit ise bu atoma nötr atom denir. Atoma elektron verilerek ya da atomdan elektron alınarak atomların yüklenmesi sağlanır. Bir atomda proton sayısı elektron sayısından fazla ise bu atomlara pozitif yüklü iyon veya katyon denir. Simgesi “+e” ile gösterilmektedir. Atomun içinde elektron sayısı çoksa dışarıdan elektron kazanmıştır. Buna negatif yüklü iyon denir ve “– e” ile gösterilir. Aynı zamanda bunlara “anyonda” denir. (aX ±b) ifadesinde; A: X atomunun atom numarasını, +b: X atomunun kaybetmiş olduğu elektron sayısını, -b: X atomunun kazanmış olduğu elektron sayısını gösterir.
Atom Ağırlığı
Farklı atomlardaki protonlarla neutronların sayısına “atom sayısı” ve “atom ağırlığı” adı verilir. Bir atom sayısı, o atomda ne kadar proton, yada elektron bulunduğunu gösterir. Bu durumda, o atomun hangi elemanının atomu olduğu anlaşılır.
İzotop Atom Nedir?
Atom numarası aynı (proton), kütle numarası farklı olan atomlara izotop (isotope) atom denir. Diğer bir ifadeyle proton sayıları aynı (p.s= A.N), nötron sayısı (K.N= p.s + n.s) farklı atomlara izotop atom denir. İzotop atomların kimyasal özellikleri aynı, fiziksel özellikleri farklıdır. Nötr olmayan, iyon halindeki izotop atomların hem fiziksel, hem kimyasal özellikleri farklıdır.
Atom Modelleri
Atomlar maddenin en küçük yapı taşı olmasına rağmen hiçbir şekilde görülemez. Gözle görülmeyen çok küçük bir parçacık olan atom ve sadece taramalı tünel mikroskobu (atomik kuvvet mikroskobu) ile incelenebilir. Maddenin kütlesi olduğu halde maddeyi meydana getiren atomların tek tek kütleleri ölçülemez ve atomlar duyu organları tarafından algılanamaz.
Geçmişten günümüze kadar atom hakkında, birçok bilim adamları deneyler yapmış ve atom hakkında edindikleri bilgileri açıklamak için çeşitli bilimsel modeller ortaya koymuşlardır. Atom hakkında ortaya konan her yeni model bir önceki modelin eksikliğini gidermiştir. Atom hakkındaki her yeni model bir önceki modelin eksikliğini tamamlamıştır. Atom hakkında yapılan yeni deneyleri açıklayamayan modelin yerine de yeni bir model geliştirilmiştir. Eski atom modellerinin bugün geçerli olmamasının sebebi, o modelleri geliştiren bilim adamlarının iyi düşünememesinden değil, o dönemde bilinenlerin bugün bilinenlere göre daha az olmasından kaynaklanır. (Dalton atom modeli açıklandığında o dönemde bilinenler dikkate alındığında o modeli geliştirmek, Bohr atom modelini geliştirmekten daha zordu).
Atom modelinin tarihsel gelişimi geçmişten günümüze atom modelinin ortaya çıkması Thomson, De Broglie, Democritus, Rutherford gibi filozof ve bilim adamlarının görüşleri sayesindedir. Günümüzde kullanılan atom modeli Modern Atom Teorileridir. Bu günümüz modeli, yeni bir model bulunmasına kadar geçerliliğini devam ettirecektir.
| M.Ö 400 | 1803-1808 | 1898 | 1908-1911 | 1913 | 1920 | 1924 | 1926 | 1933 |
| Democritus | John Dalton | John Joseph Thomson | Ernest Rutherford | Niels David Bohr | Werner Heisenberg | De Broglie | Born Heisenberg | Erwin Schrödinger |
Democritus Atom Modeli (Democritus–M.Ö. 400)
M.Ö. 400’lü yıllarda atom hakkındaki ilk görüş Teosta yaşayan Yunanlı filozof Democritus tarafından ortaya konmuştur. Democritus, maddenin taneciklerden meydana geldiğini savunmuş ve bu taneciklere atom demiştir. Democritus, atom hakkındaki görüşlerini varsayımlara göre söylemiştir. Democritus’ a göre;
- Madde parçalara ayrıldığı zaman sonunda bölünemeyen bir tanecik elde edilir ve bu tanecik atomdur.
- Bütün maddeler aynı tür atomlardan meydana gelir.
- Maddelerin farklı olmasının nedeni maddeyi oluşturan atomların sayı ve dizilişi şeklinin farklı olmasıdır.
- Atom görülemez.
- Atom görülmediği için bölünemez.
Dalton Atom Modeli (John Dalton 1766–1844)
1805 yılında Atom hakkında ilk bilimsel görüş İngiliz bilim adamı John Dalton tarafından ortaya atılmıştır. Dalton Atom teorisi;
- Maddenin en küçük yapı taşı atomdur.
- Maddeler çok küçük, bölünemez, yok edilemez berk taneciklerden meydana gelir.
- Atom parçalanamaz.
- Atom içi dolu küre biçimindedir.
- Bütün maddeler farklı cins atomlardan meydana gelmiştir. Maddeler, kimyasal bakımdan birbirleriyle aynı atomları içerir.
- Maddelerin birbirlerinden farklı olmasının nedeni maddeyi oluşturan atomların farklı özellikte olmasıdır.
- Bir maddeyi meydana getiren atomların tamamı birbirleriyle aynı özelliklere sahiptir.
- a) Madde fiziksel yada kimyasal değişmeye uğradığı zaman atomlar varlıklarını korurlar, parçalanmaz ve tekrar meydana getirilemezler.
- b) Kimyasal olaylar atomların birleşmesi yada ayrılması sonucunda meydana gelir. Atomlar birleşerek molekülleri meydana getirir. Bir bileşiğin molekülleri birbirinin aynısıdır.
- c) Dalton, maddenin yapısını açıklayan atom teorisiyle ün kazanmıştır. Gazların bazı özellikleri ile ve özellikle kısmi basınçları ile ilgili çalışmalarda bulunmuştur.
- d) Birçok elementin atom ağırlıklarını ölçmeye çalışmış ve bu ağırlıklarla ilgili bir tablo yapmıştır. Teknolojinin gelişmesiyle bilim adamları tarafından atomların ağırlıklarını tekrar ölçülmüş ve Dalton’un hazırladığı bu tablonun hatalı olduğu kanıtlanmıştır.
- e) Sabit oranlar kanunu ve katlı oranlar kanunu, bileşiklerdeki kütlesel ilişkilere bakarak 1803’ de John Dalton, maddelerin çok küçük yapı taşlarının topluluğu halinde bulunduğu, fikrini ileri sürmüştür.
- Aynı elementin atomları şekil, büyüklük, kütle bakımından aynıdır. Ancak bir elementin atomları başka bir elementin atomlarından farklıdır.
- Atomlar belli sayılarda birleşerek molekülleri oluştururlar. 1 atom X ile 1 atom Y den XY, 1 atom X ile 2 atom Y den XY2 bileşiği meydana gelir. Meydana gelen bu bileşiklerin özellikleri, moleküller topluluğudur.
- Farklı cins atomlar farklı kütlelidir.
Dalton atom teorisindeki eksiklikler şunlardır;
- Aynı cins elementlerin atomları tam olarak aynı değildir. Kütleleri farklı (izotop) olanları vardır.
- Atomlar içi boş küreler değildir. Boşluklu yapıdadır.
- Atomlar nükleer enerji ile parçalanabilir.
- Maddelerin en küçük parçasının atom olduğu ve atomların parçalanamaz olduğu doğru değildir. Radyoaktif atomlar daha küçük parçalara ayılarak daha farklı kimyasal özellikte başka atomlara ayrışabilir; proton, nötron, elektron gibi parçacıklar saçabilirler.
Thomson Atom Modeli (John Joseph Thomson 1856–1940)
İngiliz fizik bilgini Joseph Thomson, elektronlar hakkındaki çalışmalarıyla 1906 da, Nobel fizik ödülü almıştır. 1885’te içi boş bir cam tüp içerisinden elektrik akımları üzerinde çalışırken ışınları tüpün negatif (katot) kutbundan geldiğini görmüş ve ilk kez katot ışınlarını bulmuştur ve böylece elektronları da bulmuş elektronların her atomda var olan temel parçacıklar olduğunu söylemiştir.
Dalton atom modelinde (–) yüklü elektronlardan ve (+) yüklü protonlardan söz edilmemiştir. Yapılan deneyler ile; katot ışınlarından protonun varlığını ortaya koymuştur. Thomson atom altı parçacıklar üzerinde çalışmaları sırasında icatı olan katot tüpü yardımıyla 1887’de elektronu keşfinden sonra kendi atom modelini ortaya atmıştır.
Elektronların kütlesi pozitif yüklerin kütlesinden küçüktür. Bundan dolayı atomları pozitif yükler meydana getirir. Atomda elektriksel dengeyi sağlamak için pozitif yük sayısına eşit sayıda elektron küre içinde dağılmış durumdadır.
1897 yılında Thomson tarafından atomun yapısı ve özellikleri hakkında ilk model, ortaya konmuştur. Thomson atom modeli, bir karpuza veya üzümlü keke benzemektedir.
John Joseph Thomson’a göre;
- Atom küre şeklindedir. (Çapı 10–8 cm)
- Atomda (+) ve (–) yüklü tanecikler vardır.
- Thomson’a göre atom; dışı tamamen pozitif yüklü bir küre olup negatif yüklü olan elektronlar kek içerisindeki gömülü üzümler gibi bu küre içerisine gömülmüş durumdadır.
- Atomlar, daha küçük taneciklerden meydana geldiği için parçalanabilir.
Elektron’un Keşfi
Maddenin yapısına ilk olarak modern yaklaşım Thomson’un katot ışınlarını inceleyerek elektronun keşfi ile başlamıştır. Thomson: elektriksel gerilim uygulanan katot ışınları tüpünde katot ışınların negatif kutup tarafından itildiğini pozitif kutba doğru çekildiğini belirledi.
- Aynı cins elektrik yüklerinin bir birini itmesi ve farklı yük elektrik yüklerinin birbirini çekmesi sebebi ile Thomson katot ışınlarının negatif elektrik yüklerinden olduğu sonucuna vardı.
- Thomson yaptığı deneyinde katot için farklı madde kullandığında ve deney tüpünün farklı gazla doldurulduğunda da katot ışınlarının aynı davranışta olduğunu gördü. Bu durumda elektronun maddenin cinsinin karakteristik bir özelliği olmadığını bütün atom cinsleri için elektronun her birinin aynı olduğunu sonucunu ortaya koydu.
- Elektron negatif yüklü olduğu için elektriksel alanda pozitif kutba doğru sapar. Elektriksel alandaki bu sapmalar taneciğin yükü (e)ile doğru, kütlesi(m) ile ters orantılıdır. Yükün kütleye oranı (e/m) bir elektirik alanı içinde elektronların doğrusal yoldan ne kadar sapacağını gösterir.
Proton’ un Keşfi
Katot tüpleriyle elektron elde edildiği gibi, elektrik deşarj boşalma (deşarj) tüpleriyle de pozitif iyonlar elde edilir. Bu tüplerde uygulanan yüksek gerilim neticesinde atomdan elektronlar koparılarak pozitif iyonlar meydana getirilir. Bu pozitif iyonlar bir elektriksel alanda elektronun ters yönünde hareket ederek negatif elektrota (katota) doğru ilerler. Bu iyonların büyük bir bölümü hareketleri sırasında ortamdaki elektronlara çarparak nötral atomlar meydana getirirler. Az bir bölümü ise yollarına devam ederek katota ulaşırlar. Eğer ortası delikli bir katot kullanılırsa, pozitif parçacıklar delikten geçer, bu ışınlara kanal ışınlar veya pozitif iyonları denir.
- Pozitif iyonlar için e/m nin belirlenmesinde katot ışınlarının incelenmesinde kullanılan yöntemin aynısı kullanıldı. Katot ışınlarında katot maddesi ne olursa olsun elde edilen ışınların e/m oranı hep aynı idi. Oysa pozitif ışınlarda elde edilen e/m oranı tüpteki gazın oranına göre farklı olduğu bulundu.
- Elektronlar ve protonlar yüklü parçacıklardır. Bunlar yük bakımından eşit, işaretçe zıttılar. Protonlar +1 birim yüke, elektron ise –1 birim yüke eşittir.
- Nötr bir atomda proton sayısı elektron sayısına eşit olduğundan yükler toplamı sıfıra eşittir.
- Atom çapı 10-8 cm olan bir küre biçimindedir. Küre içerisinde proton ve elektronlar atomda rastgele yerlerde bulunurlar. Elektronun küre içindeki dağılımı üzümün kek içindeki dağılımına benzer.
- Elektronların kütlesi küçüktür. Bu nedenle atomun ağırlığını büyük ölçüde protonlar oluşturur.
Thomson atom teorisinin eksiklikleri;
- Nötron denilen parçacıklardan söz edilmemesi
- Proton ve elektronların atomda rastgele yerlerde bulunduğu iddiası ise teorinin hatalı tarafıdır.
Rutherford Atom Modeli (Ernest Rutherford 1871–1937)
Atomun çekirdeğini ve çekirdekle ilgili birçok özelliğini ilk kez keşfeden bilim adamı Ernest Rutherford’ dur.
- Atom kütlesinin tamamına yakını merkezde toplanır, bu merkeze çekirdek denir.
- Atomdaki pozitif yüklere proton denir.
- Elektronlar çekirdek etrafında gezegenlerin Güneş etrafında döndüğü gibi dairesel yörüngelerde devamlı dönerler. Çekirdekle elektronlar arasında çekim kuvveti olduğundan elektronların çekirdeğe düşmemeleri için dolanmaları gerekir. (Yörünge daire şeklinde değil, enerji seviyesine karşılık gelen orbitallerde dolanır).
- Elektronların bulunduğu hacim çekirdeğin hacminden çok büyüktür.
- Çekirdekteki protonların sayısı (yük miktarı) bir maddenin bütün atomlarında aynı, fakat farklı maddenin atomlarında farklıdır.
- Çekirdekteki proton (yük) sayısı, elektron sayısına eşittir.
- Çekirdekteki pozitif yüklerin kütlesi yaklaşık atom kütlesinin yarısına eşittir.
Yeni Zellanda’da doğmuş ve başarılı bir öğrenci olduğundan 1894 yılında İngiltere’ye gelmiştir. İlk önceleri elektromanyetik radyasyon hakkında çalışmalar yapmıştır. sonraları X ışınlarına ve radyoaktivite ilgisini çekmiştir. Farklı tipte elektromanyetik radyasyonların varlıklarını ortaya atmış bunlara ilk defa α,β ve γ olarak adlandırmış ve sembollendirmiştir. Devamla α ışımasının helyum çekirdeği, β ışımasının ise elektron içerdiğini bulmuş ve bu çalışmasından dolayı 1908′ de kimya Nobel ödülü almıştır. 1911 yılında atomun kütlesini içine alan çok küçük bir merkezinin olduğunu ortaya atmıştır. Rutherford bu merkeze çekirdek adını vermiştir. Ernest Rutherford atomun yapısının açıklanmasında önemli katkıları vardır.
Rutherford’dan önce Thomsan atom modeli geçerliydi. Bu modele göre atom küre biçimindedir. Küre içerisinde proton ve elektronlar bulunur. Acaba bu proton ve elektronlar atom içerisinde belli bir yere mi yoksa rastgele mi dağılım içerisinde mi bulunuyordu? Rutherford bu sorunun cevabı ve Thomson atom modelinin doğruluk derecesini anlamak için yaptığı alfa (α) parçacıkları deneyinde bir model geliştirdi.
Radyum ve polonyum bir a- ışını kaynağıdır. Rutherford bir radyoaktif kaynaktan çıkan a- taneciklerini bir demet halinde iğne ucu büyüklüğündeki yarıktan geçirdikten sonra kalınlığı 10-4 cm kadar olan ve arkasında çinko sülfür (ZnS) sürülmüş bir ekran bulunan altın levha üzerine gönderdi. Altın levhayı geçip ekran üzerine düşen a – parçacıkları ekrana sürülen ZnS üzerine ışıldama yaparlar. Böylece metal levhayı geçen a – parçacıklarını sayma olanağı elde edilebilirdi. Rutherford deneyinde metal levha üzerine gönderilen a – parçacıklarının %99,99 kadarının ya hiç yollarından sapmadan veya yollarından çok az saparak metal levhadan geçtiklerini, ama çok az bir bölümünün ise metale çarptıktan sonra büyük bir açı yaparak geri döndüklerini gördü. Rutherford sonra deneyi altın levha yerine kurşun, bakır ve platin levhalar üzerinde denedi. Tümünde de sonuç aynı çıkmıştı.
Kinetik enerjisi yüksek olan çok hızlı olarak bir kaynaktan çıkan α – parçacıklarının geriye dönmesi için;
- Metal levhada pozitif bölümün olması
- Bu pozitif yüklü bölümün kütlesinin çok büyük olması gerekir.
Rutherford’ un deneyden çıkardığı sonuç;
- Eğer α – tanecikleri atom içerisinde ki bir elektrona çarpsaydı kinetik enerjileri büyük olduğu için elektronu yerinden sökerek yoluna devam edebilirdi. Ayrıca α – taneciği pozitif, elektron olduğundan söz konusu olmaması gerekirdi. Bu düşünceyle hareket eden Rutherford metale çarparak geriye dönen α parçacıklarının sayısı metal levhadan geçenlere oranla çok küçük olduğu için atom içerisinde pozitif yüklü ve kütlesi büyük olan bu kısmın hacmi, toplam atom hacmine oranla çok küçük olmalıdır diyerek, bu pozitif yüklü kısma çekirdek dedi.
- Rutherford atomun kütlesinin ortalama çekirdeğin kütlesine eşit olduğu ve elektronlar da çekirdek etrafındaki yörüngelere döndüğünü ileri sürmüştür. Rutherford atomu güneş sistemine benzetmiştir. Rutherford atom modelini ortaya koyduğunda nötronların varlığı bilinmiyordu. Günümüzde ise çekirdeğin proton ve nötronlar içerdiği ve bunların çekirdeğin kütlesini meydana getirdiklerine inanılmaktadır. Rutherford’un atom modelinin boyutlarını anlamak önemlidir. Eğer bir atomun çekirdeği, bir tenis topu büyüklüğünde olmuş olsaydı, bu atom büyük bir stadyum büyüklüğünde olurdu.
Niels Hendrik Bohr (Niels David Bohr 1875–1962)
Bohr atom teorisi hidrojenin yayınma spektrumuna dayanılarak açıklanır.
Bohr’ a göre;
- Elektronlar çekirdek etrafında belirli uzaklıklardaki katmanlarda dönerler, rastgele dolanmazlar.
- Yüksek enerji düzeyinde bulunan elektron, düşük enerji düzeyine geçerse fotonlar halinde ışık yayarlar.
- Kararlı hallerin tamamında elektronlar çekirdek etrafında dairesel yörünge izlerler.
Danimarkalı fizikçi Niels Hendrik Bohr, doktorasını bu şehirde yapmış, 1911′ de John Joseph Thomsonla İngiltere’ye çalışmak için gitmiştir. Çalışmaları sonucunda atom spektrumları ve yapısı hakkındaki teorisini ortaya koyarak kitap olarak yayınlamıştır. Bir süre sonra Kopenhag’a dönerek, teorik fizik enstitüde yöneticilik yapmaya başlamıştır. Burada kimya ve fizik alanında Nobel ödülleri kazanan W. Heisenberg, W.Pouli ve L. Pauling gibi bilim adamları yetiştirmiştir.
İlk kuantum atom modelini önermiştir. Kuantum mekaniğinin ilk gelişmesinde aktif olarak katıldı. Çekirdek fiziğine, çekirdeğin sıvı damlası modelinin geliştirilmesinde de rolü büyüktür. 1922’de fizikte Nobel ödülünü, atomların yapısı ve atomlardan yayılan ışınım üzerine yaptığı çalışmalarından kazandı.
Şimdiye kadar anlatılan tüm atom modellerinde atomun çekirdeğinde (+) yüklü proton ve yüksüz nötronların var olduğu, çekirdeğin çevresinde dairesel yörüngelerde elektronların dolaştığı anlatıldı. Bu elektronların çekirdek çevresinde nasıl bir yörüngede dolaştığı, hızı ve momentumlarının ne olduğu ile ilgili bir sonuç ortaya konmadı. Bohr ise atom teorisinde elektronların hareketini bu noktadan inceledi.
- Bir atomdaki elektronlar çekirdekten belli uzaklıkta ve kararlı halde hareket ederler. Her kararlı halin sabit bir enerjisi vardır.
- Her hangi bir enerji seviyesinde elektronlar dairesel bir yörüngede (orbitalde) hareket eder. Bu yörüngelere enerji düzeyleri veya kabukları denir.
- Elektronlar kararlı hallerden birinde bulunurken atomdan ışık (radyasyon) yayılmaz. Ancak yüksek enerji düzeyinden düşük enerji düzeyine geçtiği zaman, seviyeler arasındaki enerji farkına eşit bir ışık kuantı yayınlar. Bunlara E=h.ν bağıntısı geçerlidir.
- Elektron hareketinin mümkün olduğu kararlı seviyeler K, L, M, N, O gibi harflerle veya en düşük enerji düzeyi 1 olmak üzere her enerji düzeyi pozitif bir tam sayı ile belirlenir ve genellikle “n” ile gösterilir. (n : 1,2,3, …∞ )
Bohr atom modeli
Günümüz atom modelimize göre : Borh atom teorisi elektronların dairesel yörüngelerde hareket ettiği, ifadesi yanlıştır.
1913’te Danimarkalı fizikçi Niels Bohr, hidrojen atomunun kuantum kuramına dayanarak açıkladı. Buna göre çekirdek çevresindeki elektron, her enerjiyi değil, ancak belirli enerjileri alabiliyordu. En düşük enerjili durumdaki atoma temel durumdaki atom, enerji verilmiş atomlara da uyarılmış atom denir. Elektron yüksek enerjili durumdan düşük enerjili duruma sıçrayarak düşer, bu sırada ışık yayınlanır. Bohr atom modeli hidrojen atomunun yanı sıra bir elektronlu helyum (+1 yüklü helyum iyonu) ve lityum iyonu (+2 yüklü lityum iyonu) tayf çizgilerine başarıyla uygulandı. Ancak Bohr atom modeli çok elektronlu atomların davranışlarını açıklayamadığından yaklaşık 12 yıl geçerli kaldı. Bununla beraber, teori çok elektronlu atom ve iyonların karmaşık tayf çizgilerini açıklamakta yetersiz kaldı ve yerini Modern atom modeli aldı.
Bohr atom teorisine göre elektronlar çekirdek belirli uzaklıklarda dairesel yörüngeler izler. Çekirdeğe en yakın yörüngede bulunan (n = 1) K tabakası en düşük enerjilidir. Çekirdekten uzaklaştıkça tabakanın yarı çapı ve kabukta bulunan elektronun enerjisi artar. Elektron çekirdekten sonsuz uzaklıktayken (n = ∞) elektronla çekirdek arasında çekim kuvveti bulunmaz. Bu durumda elektronun potansiyel enerjisi sıfırdır. Elektron atomdan uzaklaşmıştır. Bu olaya iyonlaşma denir.
Elektron çekirdeğe yaklaştıkça çekme kuvveti meydana geleceğinden, elektronun bir potansiyel enerjisi meydana gelir. Elektron çekirdeğe yaklaştıkça atom kararlı hale gelir, potansiyel enerjisi azalır. Buna göre elektronun her enerji düzeyindeki potansiyel enerjisi sıfırdan küçük olur. Yani negatif olur. Bohr, hidrojen atomunda çekirdeğe en yakın enerji düzeyinde (K yörüngesi) bulunan elektronun enerjisini –313,6 kkral/mol olarak bulmuştur.
Modern Atom Modeli (Kuantum Atom Modeli)
Günümüzde kullanılan atom modeli, modern atom teorisi sonucu ortaya konmuştur. Bu teoriye göre elektronlar çok hızlı hareket ettikleri için belirli bir yerleri yoktur. Yani elektronların bulunduğu kabuk kavramı yanlış bir kavramdır. Elektronların sadece bulunma ihtimalinin olduğu bölgeler bilinebilir ve elektronların bulunma ihtimalinin olduğu bölgelere elektron bulutu denir.
Bohr, elektronu hareket halinde yüklü tanecik olarak kabul edip, bir hidrojen atomundaki elektronun sadece bazı belirli enerjiye sahip olacağını varsayarak teorisini ortaya attı. Bu teori hidrojen gibi tek tek elektronlu He+ , Li+2 iyonlarına da uymasına rağmen, çok elektronlu atomların ayrıntılı spektrumlarının, kimyasal özelliklerini açıklanmasına uymamaktadır. Yine de modern atom modelinin gelişiminde bir basamak teşkil etmiştir.
- Atomda belirli bir enerji düzeyi vardır ve elektron ancak bu düzeyden birinde bulunur. Enerji düzeyleri “n” ile gösterilir. Bu enerji düzeylerine baş kuantum sayısı adı verilmektedir. Baş kuantum sayısı orbitallerin çekirdekten ortalama uzaklığını veya enerjisini belirler. Çekirdekten uzaklaştıkça enerji artar. Protonların elektronları çekim gücü azalır, çekim gücü azalınca elektronların hareketi ve enerjisi artmış olur.
- Elektron bir enerji düzeyindeki hareketi sırasında çevreye ışık yaymazlar.
- Atoma iki düzey arasındaki fark kadar enerji verilirse elektron daha yüksek enerji düzeyine geçer.
- Atoma verilen enerji kesilirse elektron enerjili düzeyinde kalamaz daha düşük enerji düzeyinden birine geçer. Bu sırada iki düzey arasındaki fark kadar enerjiyi ışık şeklinde çevreye verir
- Elektronlar kendi etrafında döndükleri gibi çekirdek etrafında da dönerler. Elektronun kendi ekseni çevresinde dönme hareketine spin hareketi, çekirdek etrafındaki dönme hareketine de orbital hareketi adı verilir. Çekirdek etrafında dönmeleri sırasında elektronların bulunma olasılığının yüksek olduğu geometrik yerlere orbital denir.
Modern atom modeli
Modern atom modeli dalga mekaniğindeki gelişmelerin elektronun hareketine uygulanmasına dayanır. Bu modelin öncüleri Werner Heisenberg ve Erwin Schrödlinger gibi bilim adamları bu modelin öncüleridir.
Avusturya’nın Viyana şehrinde doğan Erwin Schrödlinger (1887–1961) 1939 yılından 1956 yılına kadar İrlanda da çalışmıştır. 1926 yılında henüz İsviçre de çalışırken Heisenberg tarafından ortaya atılıp formüllendirilen kuantum teorisine alternatif olarak kendi adıyla anılan (Schrödlinger eşitliği ) dalga mekaniği teoremini ortaya atmıştır. Schrödlinger teoremi, elektronların gerek atom içerisinde gerekse moleküllerdeki hareketini dalga cinsinden matematiksel bir biçimde açıkladı. 1933’de fizik Nobel ödülünü İngiliz fizikçi Paul Dirac ile paylaştı.
Werner Heisenberg (1901 – 1976) Atomların yapısını ve elektron gibi atomaltı parçacıkların davranışlarını açıklayan kuantum mekaniği teorisinin kurucusu olan bir Alman fizikçidir. 1927’de kendi ismi ile anılan belirsizlik ilkesini ortaya atmıştır.Bu ilkesinde Heisenberg, elektron kadar küçük olan bir parçacığın hem pozisyonunu hem de momentumunu kesin olarak bulmak mümkün değildir demektedir. Bu çalışmalarından dolayı 1932’ de Nobel fizik ödülü almıştır.
1924 yılında Louis De broglie ışın ve maddenin yapısını dikkate alarak küçük tanecikler bazen dalgaya benzer özellikler gösterebilirler biçimindeki hipotezi elektron demetlerinin bir kristal tarafından X – ışınlarına benzer şekilde saptırılması ve dağılması deneyi ile ispatlandı.
1920’li yıllarda Werner Heisenberg, atomlardan küçük taneciklerin davranışlarını belirlemek için ışığın etkisini inceledi. Bunun sonucunda Heisenberg belirsizlik ilkesi olarak anılan şu sonucu çıkardı:
“Bir taneciğin nerede olduğu kesin olarak biliniyorsa, aynı anda taneciğin nereden geldiği ve nereye gittiğini kesin olarak bilemeyiz. Benzer şekilde taneciğin nasıl hareket ettiğini biliyorsak onun yerin kesin olarak bilemeyiz.”
Buna göre elektronun herhangi bir andaki yeri ve hızı aynı anda kesin olarak bilinmez. Bir taneciğin yerini ve hızını ölçebilmek için o taneciği görmek gerekir. Taneciğin görünmesi de taneciğe ışın dalgası göndermekle olur. Elektron gibi küçük tanecikleri belirlemek için düşünülen uygun dalga boyundaki ışık, elektronun yerini ve hızını değiştirir. Bundan dolayı aynı anda elektronun yeri ve hızı ölçülmez. Bu sebeple de elektronların çekirdek etrafında belirli dairesel yörüngeler izledikleri söylenemez. Yörünge yerine elektronun ( yada elektronların ) çekirdek etrafında bulunma ihtimalinden söz etmek gerekir.
Modern atom modeli atom yapısı ve davranışlarını diğer atom modellerine göre daha iyi açıklamaktadır. Bu model atom çekirdeği etrafındaki elektronların bulunma ihtimalini kuantum sayıları ve orbitaller ile açıklar.
Kuantum sayıları bir atomdaki elektronların enerji düzeylerini belirten tam sayılardır. Orbitaller ise elektronun çekirdek etrafında bulunabilecekleri bölgelerdir.
Elektron tanecik olarak düşünüldüğünde; orbital, atom içerisinde elektronun bulunma olasılığı en yüksek bölgeyi simgeler.Elektron maddesel bir dalga olarak düşünüldüğünde ise; orbital elektron yük yoğunluğunun en yüksek olduğu bölgeyi simgeler. Yani, elektron tanecik olarak kabul edildiğinde elektronun belirli bir noktada bulunma ihtimalinden, dalga olarak kabul edildiğinde ise elektron yük yoğunluğundan bahsedilir.
De Broglie Atom Teorisi
Bohr’ın atom modeli elektronların yörüngeler arası geçişlerinin mümkün kılan enerji ( kuantum ) sıçramalarını açıklayamamıştı. Bunun çözümü Fransız fizikçi Prens Victor De Broglie tarafından teklif edilmişti. De Broglie bilinen bazı taneciklerin uygun şartlarda aynı elektromanyetik radyasyonlar gibi bazen de elektromanyetik radyasyonlara uygun koşullarda aynı birer tanecik gibi davranacaklarını düşünerek elektronlara bir sanal dalganın eşlik ettiğini öne sürdü ve bir model teklif etti. Model de farklı elektron yörüngeleri çekirdeğin çevresinde kapalı dalga halkaları meydana getirmekteydi.
Born Heisenberg’ in Atom Teorisi
Almanyalı kuramsal bir fizikçi olan Born Heisenberg’in prensibini katlamakla beraber bir takım ihtimal ve istatistiki hesaplar sonucunda bir elektronun uzaydaki yerini yaklaşık olarak Born Schrödinger’in dalga mekaniği ile quantum teorisi arasında bir bağıntı kurdu. Böylece elektronun uzayın bir noktasında bulunması olasılığının hesaplanacağını göstermiş oldu.
Atomun Tarihçesi
Atom Yunancada bölünemez anlamına gelen atomustan türemiştir. Atomun tarihi; MÖ 440’lı yıllara dayanmaktadır. MÖ 440′ da Demokritos modern atom teorisini ortaya atmıştır. Kimyasal reaksiyonlarda maddenin belirlenen oranda tepkimeye girdiğini, maddelerin atom denen sayılabilen fakat bölünmez parçalardan meydana geldiğini söylemiştir. Ayrıca atomların kütlelerini gösteren bir de tablo hazırlamıştır.
Atom teorisi İngiliz kimya bilgini Jonh Dalton’ dur.
1896 yılında, Fransız bilgini Henri Becquerel (1852 – 1908) doğal radyoaktivite keşfetti. 1898 yılında da Marie ve Pierre Curie radyomu buldular. 1900’de, Alman bilgini Max Planck (1858 – 1947) Quantum Teorisi’ni ortaya attı. 1905 yılında ise büyük kuramsal fizik bilgini Albert Einstein, İzafiyet (Relativite) Teorisi’ni ortaya atarak E = mc² formülünü buldu. Rutheford 1904 yılında Alfa zerreciklerini keşfetti; 1911’de de atom çekirdeği kuramını ortaya attı.
1912 – İzotop Teorisi, Frederick Solddy (İngiltere).
1913 – Atom Yapısı Teorisi, Niels Bohr (Danimarka).
1919 – İlk Yapay Atom Paraçalanması (Rutheford azot atomunun çekirdeğini parçaladı).
1926 – Dalga Mekaniği Teorisi, Ervin Scheodinger (Almanya).
1928 – Kuantum Mekaniği Teorisi, P. A. Dirac (İngiltere).
Faydalı bilgiler : Kablo Seçim Cetveli | PLC | HMI | SCADA | Endüstri 4.0 | Servo motor | AC motor | Step motor | DC motor | Loadcell | Konveyör | Profinet | Direnç değeri okuma |







Yorum Yok